近日,微生物技术国家重点实验室(研究院)卞小莹教授课题组、武大雷教授课题组与张友明教授课题组联合攻关,在非核糖体脂肽生物合成与工程化方面取得突破。相关研究成果以“Engineering and Elucidation of the Lipoinitiation Process in Nonribosomal Peptide Biosynthesis”为题,在线发表于Nature Communications(中科院一区,五年IF=13.611)。微生物技术国家重点实验室博士研究生钟林、刁晓彤和2020届硕士毕业生张娜为该文章共同第一作者,卞小莹教授、武大雷教授和张友明教授为论文共同通讯作者,山东大学微生物技术国家重点实验室为第一作者单位和通讯作者单位。
非核糖体脂肽是一类重要的天然产物,如链霉菌来源的达托霉素和类芽孢杆菌来源的多粘菌素被认为是对抗革兰氏阳性菌和阴性菌感染的最后一道防线。脂肽类化合物的N端脂肪酸链可以进入细菌细胞膜的磷脂双分子层,对脂肽的生物活性和毒性具有重要的影响。因此,改变N端脂肪酸链可提高脂肽的成药属性,如达托霉素的创制。目前,改变其脂肪酸链主要依靠半合成法或改变脂肪酸前体供应等方法,相对复杂且产量较低。
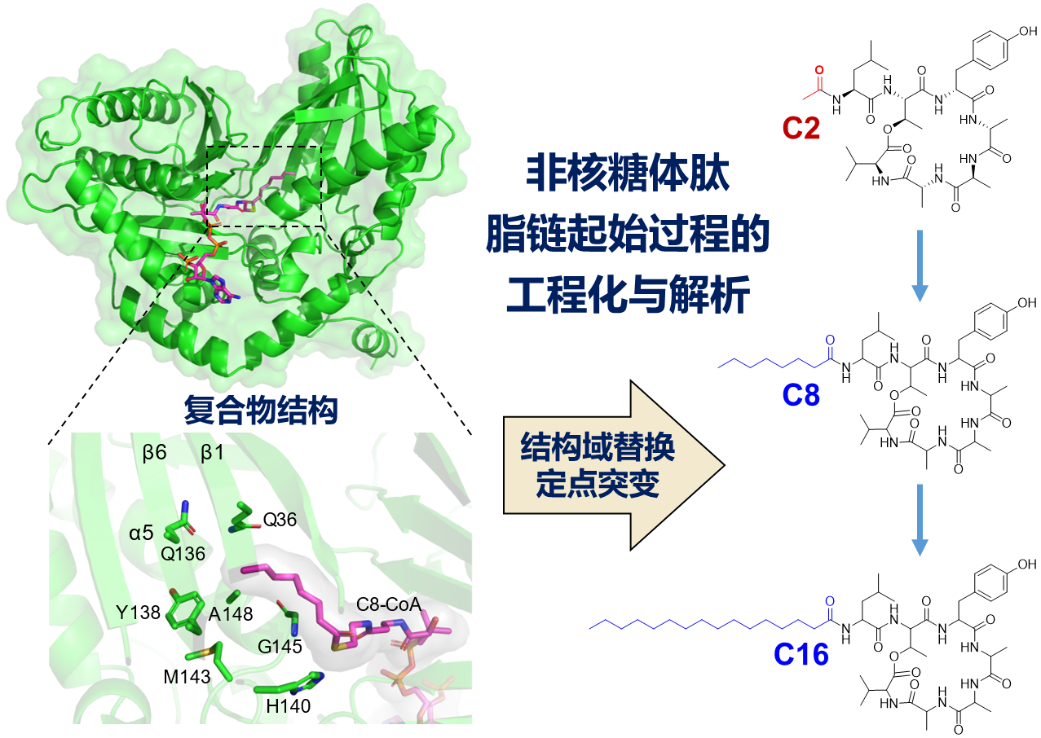
课题组前期在一株伯克氏菌中通过基因簇激活发现了两类含有不同长度脂肪酸链的脂肽rhizomide和holrhizin。它们负责装载脂肪酸的Cs结构域,具有很高的同源度,但是其装载的脂肪酸链长度却有较大差异 (C2 vs C8)。作者首先利用Cs结构域交换发现能够成功改变两类脂肽的脂肪酸链,确立了一种改变脂肽的脂肪酸链的遗传学方法。并进一步将全长Cs结构域交换的方法应用于Glidobactin A的脂链改造,也成功获得了脂肪酸链改变的衍生物,证明了该策略具有较好的普适性。
进而,通过筛选Cs结构域突变体与底物的结合能力,首次成功获得了Cs结构域与供体底物辛酰辅酶A的共结晶结构,结合关键位点的氨基酸突变,并进一步确定了负责脂肪酸链长度的其它关键氨基酸,实现了rhizomide的脂肪酸链长度从乙酰基到十六烷酰基(C2 - C16)的巨大改变,产生并鉴定了一系列的非天然脂肽。该研究通过Cs结构域替换和关键氨基酸突变为非核糖脂肽的脂肪酸链改造提供了可行的策略和较为普适的方法。为复杂脂肽的组合生物合成和工程化改造奠定了理论和实践基础。
作者同时也获得了Cs结构域与供体底物辛酰辅酶A及受体底物模拟物的三元复合物结构,发现反应中心组氨酸对两底物均具有稳定定位的作用。同时基于获得的多种不同构象的Cs结构域的精细结构,提出其在催化脂链起始过程中存在的“从底物结合到产物释放”动态结构变化模型,进一步揭示了Cs结构域的催化机理。本研究为复杂脂肽类天然产物的优化改造提供了新的方法和策略。
该项研究工作得到了国家重点研发计划、国家自然科学基金、山东省杰出青年基金、泰山青年学者项目、江苏省青年基金和山东大学齐鲁青年学者与山东大学青年交叉科学创新群体等项目的资助。山东大学生命环境研究公共技术平台和上海同步辐射光源为本工作提供了重要支持。
文章链接:https://www.nature.com/articles/s41467-020-20548-8