近日,微生物技术国家重点实验室卞小莹教授课题组在生物技术领域权威期刊Biotechnology Advances (一区,5年IF为18.248)在线发表了题为“Microbial Chassis Engineering Drives Heterologous Production of Complex Secondary Metabolites”的综述性论文(Biotechnol. Adv., 2022; 59:107966. doi: 10.1016/j.biotechadv.2022.107966),综述了近年来通过工程化改造微生物底盘实现复杂次级代谢产物高效异源表达领域的进展。山东大学微生物技术国家重点实验室为第一作者单位和通讯作者单位。
基因组测序发现隐秘次级代谢产物(天然产物)生物合成基因簇的数量远远超过迄今已知的次级代谢产物,将次级代谢产物基因簇导入适用的底盘细胞中进行异源表达以提高目标化合物的产量或促进新型化合物的挖掘逐渐成为天然产物合成生物学和绿色生物制造的核心策略。大肠杆菌和酿酒酵母作为并驾齐驱的传统模式微生物底盘,经过改造已作为微生物细胞工厂应用于许多化学品和次级代谢产物的生产,但在复杂次级代谢产物的异源表达方面仍然存在无法突破的瓶颈。在过去十年间,诸如芽孢杆菌、链霉菌、假单胞菌、伯克氏菌、粘细菌、耶罗维亚酵母以及曲霉等非模式微生物,因其代谢网络或/和生物合成方面的独特优势而得到了愈加广泛的关注。与此同时,尖端的合成生物学技术与元件的快速发展引领了非模式微生物中多样化的遗传操作,使通过新颖的微生物改造策略对宿主机进行生理表型优化或特定复杂次级代谢产物的高效异源生产成为可能。
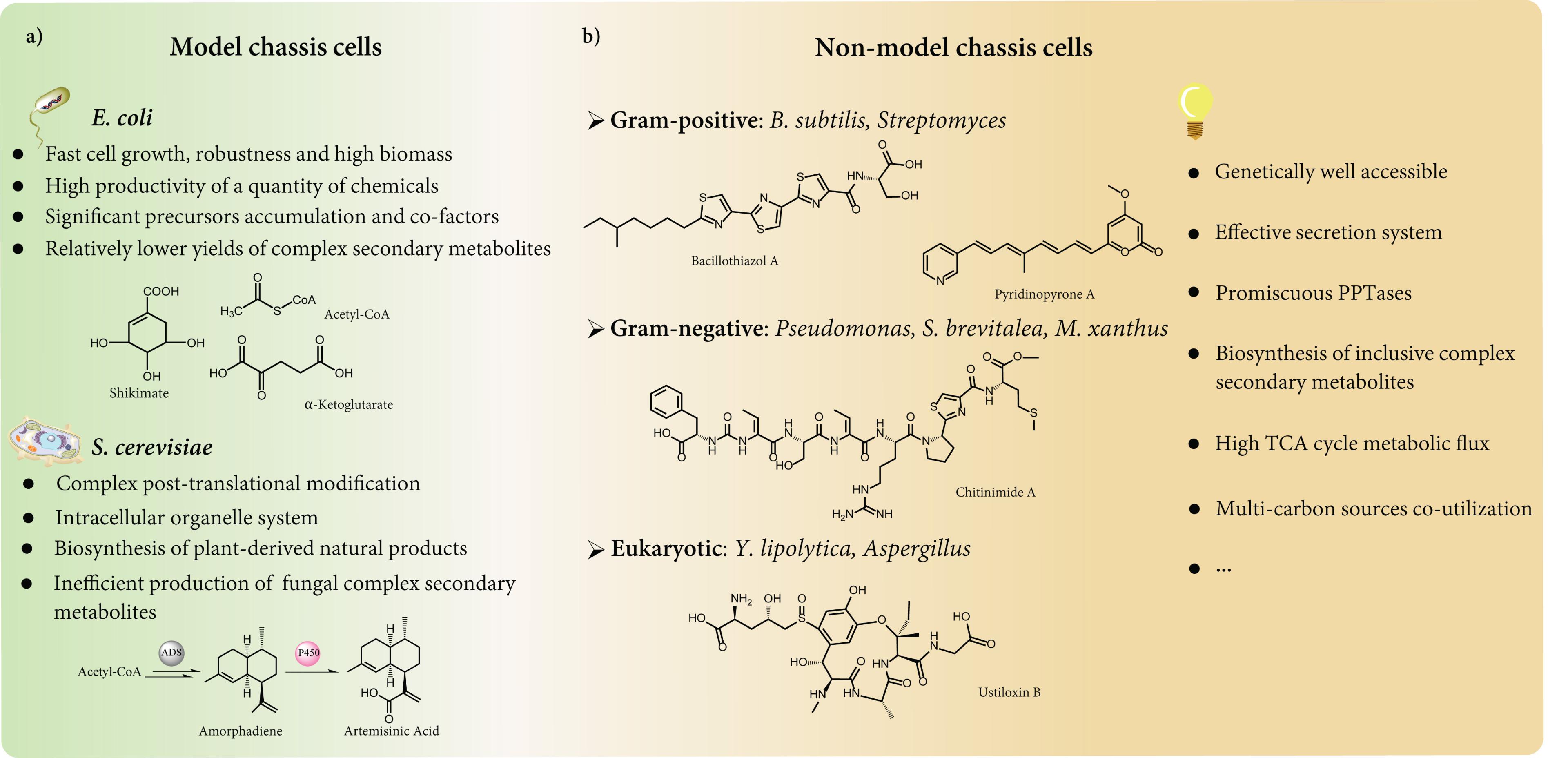
本篇论文概述了两个模式微生物底盘和一系列非模式微生物底盘的特性。鉴于当前生物合成研究和工业生产需要更多可程式化的异源宿主,更广泛的非模式微生物底盘细胞亟待构建,非模式底盘的建立将极大促进微生物次级代谢产物的挖掘、改造与高产研究。本文着重论述了近年来实现非模式微生物底盘优化的合成生物学工具以及改造策略方面的前沿进展,尤其是在对于许多复杂次级代谢产物,比如聚酮类、非核糖体多肽类和核糖体后修饰多肽类的高效异源生产方面的成功应用。最后,该论文对底盘细胞的前景进行了展望,以期在人工智能驱动的基因组时代获得高效且环境友好的细胞工厂,从而推动天然产物生物合成与绿色生物制造领域的发展。
课题组博士研究生刘嘉琪为该论文第一作者,卞小莹教授为通讯作者,张友明教授、王雪研究员和代广知博士也对该论文有重要贡献。该项工作得到了国家重点研发计划、国家自然科学基金、山东省杰青基金等项目的资助。
全文链接:https://www.sciencedirect.com/science/article/pii/S0734975022000623

